Noticias
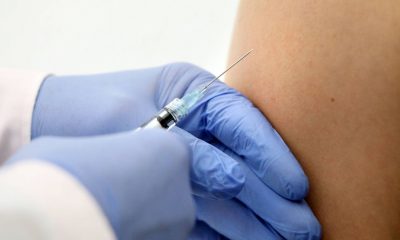
Butantan entrega documentos para a aprovação da Coronavac em crianças de 3 a 6 anos

O Instituto Butantan de São Paulo entregou nesta quarta (1º) à Agência Nacional de Vigilância Sanitária (Anvisa) os documentos solicitados em abril para a autorização da vacina Coronavac em crianças de 3 a 6 anos. À época, a Anvisa pediu ao Butantan esclarecimento de seis pontos sobre a proteção, efetividade, imunogenicidade, segurança e dados atualizados sobre a fase três de estudos clínicos em países que já aplicam o imunizante nessa população. A Anvisa vai realizar reunião com representantes de Sociedades Médicas na próxima quarta-feira (8) para discutir os documentos.
De acordo com o Instituto Butantan, não há mais pendências relativas aos estudos da Coronavac com a Anvisa. O primeiro pedido de aprovação da Coronavac para crianças e adolescentes foi realizado em julho de 2021, mas rejeitado em agosto. Na época, a Anvisa cobrou estudos de fase 3, que demonstram a eficácia da vacina.
Em dezembro de 2021, o Instituto Butantan pediu novamente a aprovação da Coronavac para a população entre 3 e 11 anos, aprovado em janeiro de 2022, mas apenas para crianças de 6 a 11 anos. A agência considerou que não havia dados suficientes para a aprovação do imunizante em crianças menores.
A demora de quase um ano para a aprovação da Coronavac para crianças de 3 a 6 anos é um exemplo da inação do Ministério da Saúde, de acordo com Claudio Maierovitch, ex-presidente da Anvisa e vice-presidente da Associação Brasileira de Saúde Coletiva (Abrasco). Ele explica que a agência precisa ter segurança para aprovar novas vacinas e medicamentos.
“A aprovação depende de dados confiáveis de segurança, eficácia, qualidade e monitoramento do fármaco”, explica Maierovitch. O grande ausente desse processo todo, desde o início, foi o Ministério da Saúde”, diz.
Fonte: Brasil de Fato
https://open.spotify.com/episode/0EFi7yPmYRoFAhRE9jC6uT
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásMP investiga projeto da Prefeitura de Iguatu e vê possível “promoção sem concurso” para motoristas da saúde
-

 Ceará3 semanas atrás
Ceará3 semanas atrásEspetáculo “Quando as Máquinas Param” promove discussão sobre violência doméstica nas cozinhas das periferias de Fortaleza
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásMinistério Público Investiga Uso de Garis da Prefeitura em Evento Privado em Iguatu
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásJustiça determina prazo para Município regularizar repasses dos consignados; SPUMI segue vigilante
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásJustiça impede exoneração em massa de ACS e ACE em Iguatu e reconhece validade dos vínculos de 2019
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásCiro e o Preço da Aliança: O Ceará Vai Cobrar as Contradições?
-

 Iguatu3 semanas atrás
Iguatu3 semanas atrásALERTA NA CÂMARA: Jurídico do SPUMI analisa riscos no PL 036 que, supostamente, pode impactar salários, anuênios e insalubridade em Iguatu
-

 Esportes3 semanas atrás
Esportes3 semanas atrásIguatu assegura classificação antecipada para a segunda fase da Série D