Brasil
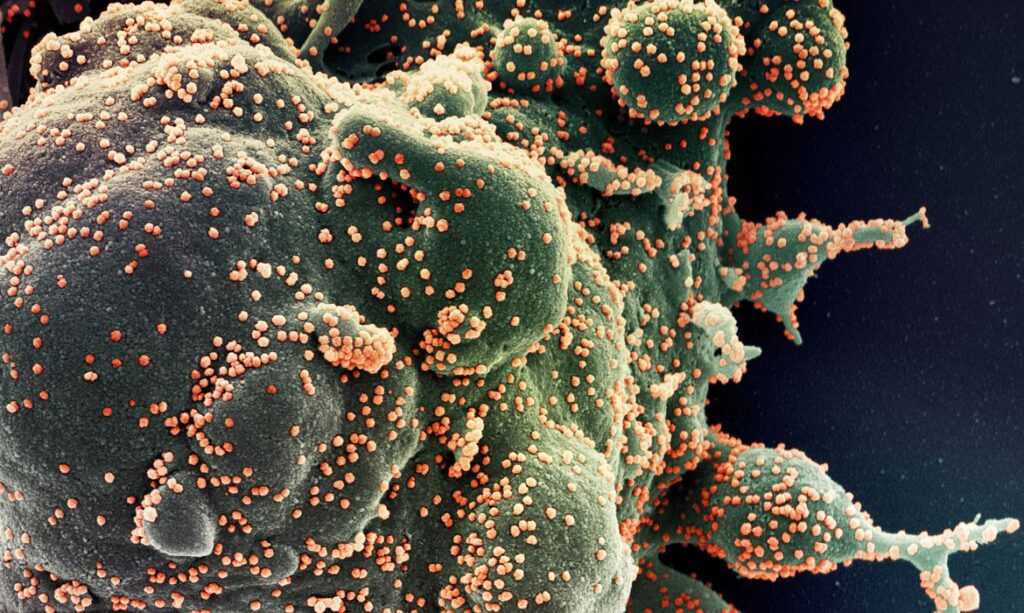
Falta de recursos e estrutura atrasam as 16 vacinas em estudo no Brasil
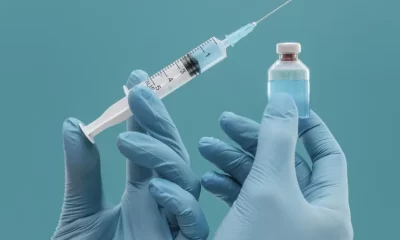
As três vacinas contra a Covid-19 aprovadas até o momento para uso no Brasil têm origem estrangeira. O imunizante mais recente a conseguir o sinal verde foi o produzido pela americana Pfizer em parceria com a alemã BioNTech. As empresas ainda não fecharam um contrato de venda para o país.
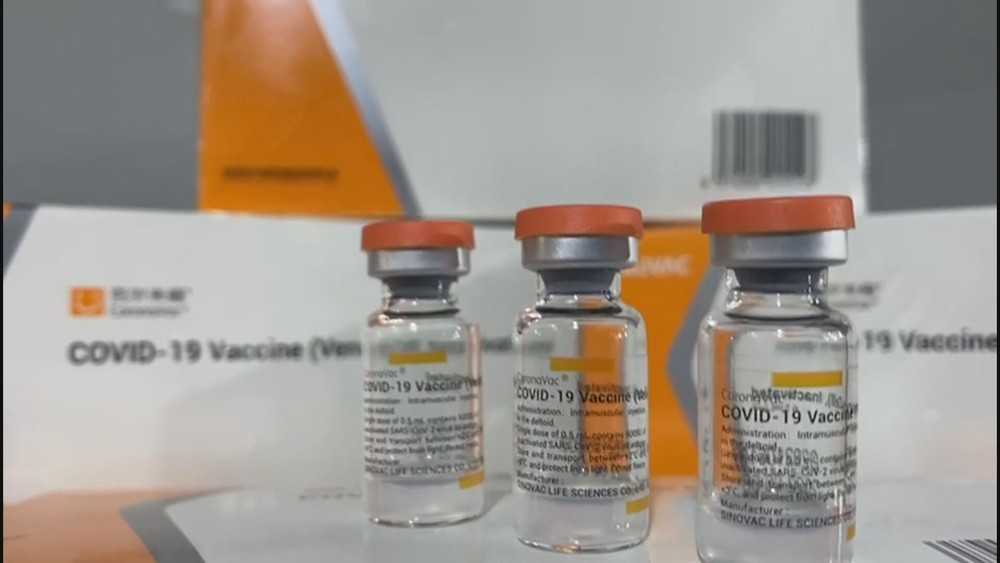
As outras duas são a Coronavac, desenvolvida pela farmacêutica chinesa Sinovac, e o imunizante da AstraZeneca, produzido pela Universidade de Oxford em parceria com a multinacional inglesa. Ambas já estão sendo utilizadas em uso emergencial autorizado pela Anvisa e em parceria com entidades brasileiras, o Instituto Butantan e a Fundação Oswaldo Cruz (Fiocruz), respectivamente.
Na corrida mundial pela imunização, o Brasil também busca produzir sua própria vacina. De acordo com um relatório do Ministério da Saúde, o país tem 16 imunizantes em fase pré-clínica de desenvolvimento. Trata-se de uma etapa ainda inicial, que indica uma dificuldade para que alguma destas vacinas possa ser aplicada ainda em 2021.
Na avaliação do imunologista Eduardo Nolasco, além dos próprios prazos do processo de desenvolvimento, o Brasil enfrenta o obstáculo estrutural: as fábricas de vacina existentes no país estão comprometidas com as produções da Coronavac e da vacina de Oxford.
“É bem provável que essa vacina brasileira tenha que esperar porque a gente não tem outro local para fazer esse desenvolvimento e realizar o teste em humanos”, afirmou.
Nolasco acredita que o ensaio clínico em humanos possa começar no segundo semestre deste ano. Para que isso aconteça, no entanto, será necessário um investimento por parte do governo federal ou da iniciativa privada.
A largada das pesquisas
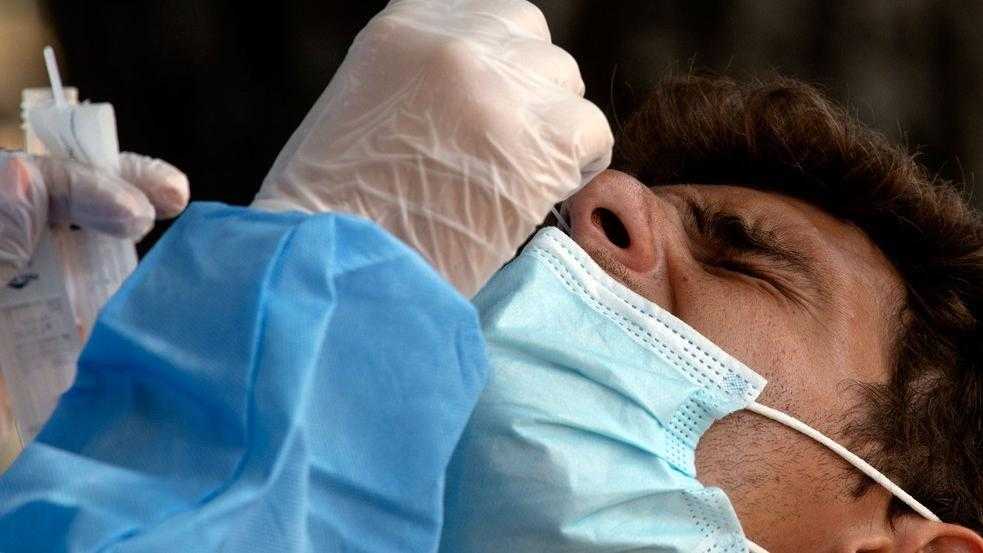
Na Pesquisa Clínica, antes de serem realizados os testes em seres humanos, há uma fase de investigação dos aspectos de segurança da medicação, com experimentações em animais. Essa fase é conhecida como etapa pré-clínica. O objetivo é obter informações preliminares sobre a atividade farmacológica do medicamento.
Segundo a Agência Nacional de Vigilância Sanitária, mais de 90% das substâncias estudadas nesta fase são eliminadas devido à toxidade aos humanos ou ineficiência terapêutica.
Quando a medicação é aprovada nos testes pré-clínicos, ela está pronta para ser aplicada e estudada em seres humanos. O procedimento científico é então dividido e classificado em quatro fases sequenciais, que têm a função de acumular dados sobre como o corpo humano responde ao novo medicamento.
Fonte: CNN Brasil
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásMP investiga projeto da Prefeitura de Iguatu e vê possível “promoção sem concurso” para motoristas da saúde
-

 Ceará3 semanas atrás
Ceará3 semanas atrásEspetáculo “Quando as Máquinas Param” promove discussão sobre violência doméstica nas cozinhas das periferias de Fortaleza
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásMinistério Público Investiga Uso de Garis da Prefeitura em Evento Privado em Iguatu
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásJustiça determina prazo para Município regularizar repasses dos consignados; SPUMI segue vigilante
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásJustiça impede exoneração em massa de ACS e ACE em Iguatu e reconhece validade dos vínculos de 2019
-

 Iguatu4 semanas atrás
Iguatu4 semanas atrásCiro e o Preço da Aliança: O Ceará Vai Cobrar as Contradições?
-

 Iguatu3 semanas atrás
Iguatu3 semanas atrásALERTA NA CÂMARA: Jurídico do SPUMI analisa riscos no PL 036 que, supostamente, pode impactar salários, anuênios e insalubridade em Iguatu
-

 Esportes3 semanas atrás
Esportes3 semanas atrásIguatu assegura classificação antecipada para a segunda fase da Série D